Tin Tức Chuyên Ngành
Tìm hiểu HNO3 – Axit Nitric: Tính chất, điều chế, ứng dụng
HNO3 hay axit nitric là hóa chất vô cơ được sử dụng trong các thí nghiệm học học, ứng dụng rộng rãi trong đời sống. Vậy axit HNO3 có gì đặc biệt, tính chất như thế nào? Cần lưu ý gì khi sử dụng và bảo quản hóa chất này? Cùng Đình Hải Plastic xem thông tin chi tiết trong bài viết dưới đây nhé!

HNO3 (Axit Nitric) là gì?
Axit Nitric là loại axit vô cơ có công thức hóa học là HNO3, chất này thường không màu, bốc khói mạnh khi ở trong không khí có độ ẩm cao. Trong tự nhiên, HNO3 thường được tạo ra từ những đợt sấm chớp, mưa sét và có trong những cơn mưa axit. HNO3 để lâu trong không khí sẽ bị chuyển màu vàng do sự tích tụ của nito oxi; có tính nguy hiểm cao, độc và ăn mòn tốt. Nếu dung dịch có hơn 86% axit nitric thì chúng được gọi là axit nitric bốc khói với khói màu trắng hoặc khói đỏ phụ thuộc vào lượng một lượng nito dioxit.
Cấu tạo phân tử HNO3
HNO3 có cấu tạo phân tử từ 1 nguyên tử hidro, 3 nguyên tử oxi và 1 nguyên tử nitơ. Trong đó nitơ có số oxi hóa cao nhất +5; hóa trị IV. Cấu tạo phân tử của loại axit này như sau:
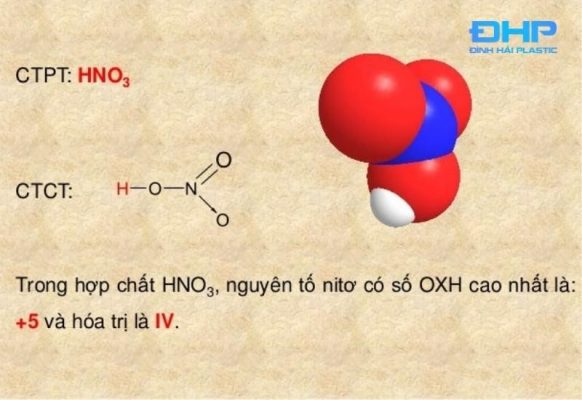
Cấu tạo phân tử Axit Nitric
Tính chất vật lí acid nitric
Để hiểu rõ hơn HNO3, chúng tôi xin cung cấp thông tin chi tiết về tính chất vật lý của hóa chất này như sau:
| Công thức hóa học | HNO3 |
| Khối lượng phân tử | 63.012 g · mol −1 |
| Ngoại quan | Chất lỏng bốc khói không màu, vàng hoặc đỏ |
| Mùi | Vị chát, ngột ngạt |
| Tỷ trọng | 1,51 g cm 3 , 1,41 g cm 3 [68% w / w] |
| Độ nóng chảy | −42 ° C (−44 ° F; 231 K) |
| Điểm sôi | 83 ° C (181 ° F; 356 K) dung dịch 68% sôi ở 121 ° C (250 ° F; 394 K) |
| Độ hòa tan trong nước | Hoàn toàn có thể trộn được |
| Áp suất hơi | 48 mmHg (20 ° C) |
| Độ axit (p K a ) | −1.4 |
| Cơ sở liên hợp | Nitrat |
| Chỉ số khúc xạ ( n D ) | 1.394 (16,5 ° C) |
| Khoảnh khắc lưỡng cực | 2,17 ± 0,02 D |
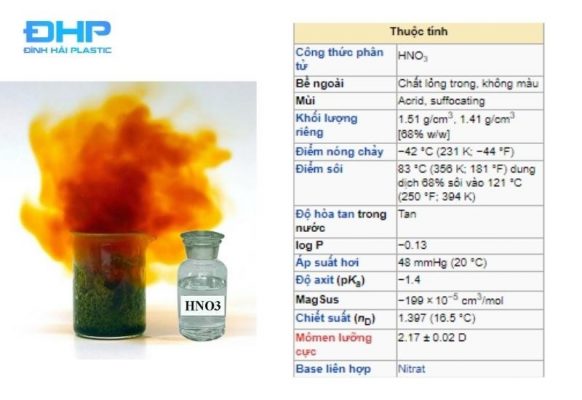
Axit HNO3
Tính chất hóa học của axit nitric
Axit nitric là một monoaxit mạnh, tính oxi hóa cao với khả năng nitrat hóa nhiều hợp chất vô cơ khác nhau. Sau đây là các tính chất hóa học nổi bật, đặc trưng của hóa chất này:
- Là axit mạnh, đặc trưng với khả năng làm quỳ tím hóa đỏ
- Có khả năng phân ly trong dung dịch, phân ly hoàn toàn thành các ion NO3- và 1 proton hydrat (hay ion hidroni)
H3O+ HNO3 + H2O → H3O+ + NO3–
- Tác dụng với oxi bazo, bazo, muối cacbonat để tạo ra muối nitrat
2HNO3 + CuO → Cu(NO3)2 + H2O
2HNO3 + Mg(OH)2 → Mg(NO3)2 + 2H2O
2HNO3 + CaCO3 → Ca(NO3)2 + H2O + CO2
- Tác dụng với hầu hết kim loại trừ Au và Pt để tạo thành muối nitrat và nước:
Kim loại + HNO3 đặc → muối nitrat + NO + H2O ( to)
Zn + HNO3 → Zn(NO3)2 + NO + H2O
Kim loại + HNO3 loãng → muối nitrat + NO + H2O
Ca + HNO3 loãng → Ca(NO3)2+ NO + H2O
Kim loại + HNO3 loãng lạnh → muối nitrat + H2
Mg(rắn) + 2HNO3 loãng lạnh → Mg(NO3)2 + H2 (khí)
- HNO3 đặc nguội không tác dụng với nhôm, sắt, crom do lớp oxi kim loại giúp bảo vệ không bị oxi hóa thêm
- Tác dụng với phi kim (các nguyên tố á kim trừ silic, halogen) tạo thành NO2 nếu là axit HNO3 đặc và NO với axit loãng và nước, oxit phi kim.
C + 4HNO3 đặc → 4NO2 + 2H2O + CO2
P + 5HNO3 đặc → 5NO2 + H2O + H3PO4
3C + 4HNO3 loãng → 3CO2 + 4NO + 2H2O
- Tác dụng với oxit bazo, bazo, muối nhưng chưa lên hóa trị cao nhất
FeO + 4HNO3 → Fe(NO3)3 + NO2 + 2H2O
FeCO3 + 4HNO3 → Fe(NO3)3 + NO2 + 2H2O + CO2
- Phản ứng với hợp chất khác nhau
3H2S + 2HNO3 (>5%) → 3S + 2NO + 4H2O
PbS + 8HNO3 đặc → PbSO4 + 8NO2 + 4H2O
Ag3PO4 tan trong HNO3
HgS không tác dụng với HNO3.
- Phản ứng với các hợp chất hữu cơ khác nhau, ăn mòn cao và vô cùng nguy hiểm
Điều chế axit nitric (HNO3)
Hiện nay tùy vào mục đích, phạm vi sử dụng mà người ta có những phương pháp điều chế HNO3 như sau:
Trong phòng thí nghiệm
Cách 1:
Sử dụng muối natri nitrat tác dụng với axit H2SO4 đặc và trăng cất ở nhiệt độ 83 độ C đến khi hỗn hợp còn lại kết chất màu trắng. PTPƯnhư sau:
H2SO4 đặc + NaNO3(tinh thể) HNO3+ NaHSO4
HNO3 bốc khói đỏ được thu có thể chuyển thành axit nitric màu trắng
Cách 2:
Phân hủy nhiệt đồng II nitrat để tạo ra nitơ dioxide và oxi, tiếp tục cho chất bày tác dụng với nước để tạo ra axit HNO3:
2Cu(NO3)2 + 2CuO + 4 NO2 + O2
4 NO2+ O2 + HNO2 +HNO3
Trong công nghiệp
Đối với các mục đích sử dụng khác nhau, axit nitric được sản xuất với các nồng độ khác nhau trong khoảng từ 52-68% theo công nghệ Ostwald. Trong đó, axit nitric loãng có thể cô đặc lên 68% với 1 hỗn hợp azeotropic và 32% nước. Nâng cao nồng độ axit bằng cách chưng cất với H2SO4 với vai trò làm chất khử thu lại nước. Quy trình thực hiện được mô tả qua chuỗi phản ứng sau:
4NH3 + 5O2 → 4NO + 6H2O (Pt, 850oC)
2NO + O2 → NO2
4NO2 + O2 + 2H2O → 4HNO3
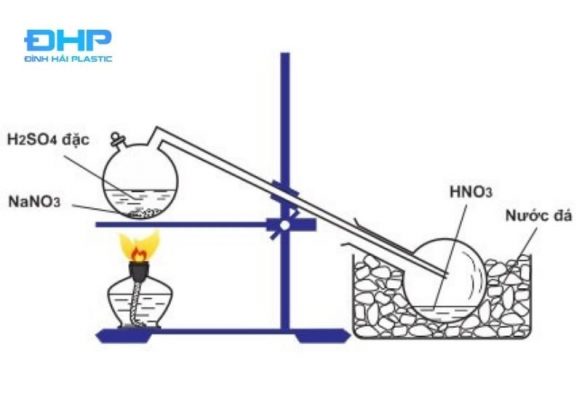
Điều chế axit nitric
Ứng dụng và vai trò của HNO3
Axit nitric là hóa chất mạnh, có khả năng tác dụng với nhiều chất khác nên có tính ứng dụng đa dạng. Sau đây là các ứng dụng của loại axit này trong đời sống:
Trong phòng thí nghiệm
- Sử dụng với vai trò là chất oxi hóa mạch, dùng làm thuốc thử cho quá trình nitrat hóa.
- Dùng trong các thí nghiệm để thử Clorit. Cho HNO3 tác dụng với mẫu thử sau đó thêm bạc nitrat để nhận biết gốc Clorua khi tạo thành bạc clorua với kết tủa trắng.
Trong công nghiệp
- Sử dụng để chế tạo thuốc nổ với HNO3 68%
- Làm các chất nền để kiểm tra độ tồn các kim loại trong dung dịch với HNO3 nồng độ thất từ 05-2%.
- Ứng dụng trong các ngành công nghiệp luyện kim, xi mạ, tinh lọc; cho HNO3 kết hợp với HCl để tạo thành nước cường toan có thể hoà tan bạch kim, vàng.
- Dùng để sản xuất các chất hữu cơ, chất bột, sơn, màu, thuốc nhuộm, thuốc tẩy,…
- HNO3 tham gia vào quá trình sản xuất nitrobenzen – chất qua trọng trong sản xuất bọt xốp polyurethane, sợi aramid và dược phẩm
- Axit nitric khoảng 10% dùng để nhân tạo thông, maple với màu vàng xám giống gỗ
- Ứng dụng để sản xuất các chất kết dính, chất bịt kín, bọc phủ, chất đàn hồi
- Hóa chất còn được dùng để sản xuất các loại phân bón như phân đạm, các muối nitrat ngành phân bón như KNO3, Ca(NO3)2,…
- Dùng làm một số loại hóa chất tẩy rửa đường ống, bề mặt kim loại, loại bỏ các tạp chất đồng thời cân bằng lại độ tiêu chuẩn của nước,…

Một số ứng dụng của HNO3
Mức độ nguy hiểm của axit nitric
Thực chất, HNO3 là loại axit vô cùng độc hại, nó gây ảnh hưởng trực tiếp tới sức khỏe con người với các mức độ như sau:
- Hít phải HNO3: Gây tổn thương cho hệ hô hấp, dẫn đến sưng phổi
- Nuốt phải axit nitric: Bỏng cùng miệng, họng, thực giản, dạ dày, bị nôn ói, tiêu chảy và có thể ảnh hưởng trực tiếp tới tính mạng con người.
- Tiếc xúc với mắt: Tổn thương giác mạc, ảnh hưởng đến thị giác hoặc nặng hơn có thể gây mù lòa.
- Tiếp xúc với da: Bỏng da nghiêm trọng nếu nồng độ cao
- Phơi nhiễm lâu gây nên các bệnh ung thư nguy hiểm.
Những lưu ý khi sử dụng axit nitric
Với những ảnh hưởng tiêu cực đối với sức khỏe con người như trên, khi sử dụng axit nitric bạn cần thực sự cẩn trọng để tránh mang lại các hậu quả, sự cố đáng tiếc xảy ra. Dưới đây là 1 số lưu ý người dùng cần ghi nhớ:
- Không sử dụng với các chất cyanit, bột kim, turpentine vì có thể dẫn đến phản ứng phát nổ hoặc tự bốc cháy.
- HNO3 ở nồng độ cao tác dụng với protein keratin gây bỏng da vì vậy bạn cần trang bị đầy đủ dụng cụ, trang thiết bị bảo hộ khi tiếp xúc với hóa chất như găng tay, kính mắt, khẩu trang, ủng, quần áo dài tay,…
- Dễ gây cháy với kim loại vì vậy cần thận trọng khi sử dụng đồng thời quan tâm đến nồng độ của axit, liều lượng sử dụng.
- Khi pha loãng HNO3 để trở về nồng độ thấp hơn cần cho axit từ từ vào nước tránh làm theo chiều ngược lại khiến axit bắn ra ngoài nguy hiểm.

Lưu ý khi sử dụng axit nitric
Bảo quản hóa chất đúng cách
Nếu bạn đang cần sử dụng hóa chất phục vụ trong phòng thí nghiệm hoặc các mục đích khác như sản xuất công nghiệp thì cần đặc biệt lưu ý các vấn đề về bảo quản HNO3. Chúng có thể tác dụng với rất nhiều loại hợp chất vô cơ, hữu cơ, vì vậy cần:
- Bảo quản axit kỹ càng trong các thùng chứa chuyên dụng, điển hình là ibc tank 1000l. Loại thùng này được sử dụng rộng rãi để đựng hóa chất nhờ khả năng chống ăn mòn, kháng hóa chất, không làm biến tính, làm từ nhựa HDPE nên rất an toàn cho sức khỏe con người. Lưu ý cần ghi tem mác rõ ràng để đánh dấu loại hóa chất, tránh nhầm lẫn khi sử dụng
- Không gian lưu trữ cũng cần được đặc biệt quan tâm đặc biệt trong các kho hóa chất riêng, nền nhà có khả năng chống hóa chất, thoái mát, tránh xa các nguồn nhiệt cũng như các chất dễ gây cháy nổ.

Sử dụng tank ibc để bảo quản hóa chất
Có thể nói, HNO3 là axit vô cùng hữu dụng trong đời sống, tham gia vào quá trình sản xuất nhiều vật liệu, sản phẩm khác nhau nhằm phục vụ mục đích của người dùng. Tuy nhiên cần lưu ý sử dụng cũng như bảo quản hóa chất đúng cách để tránh ảnh hưởng đến sức khỏe con người. Các bạn có thể mua IBC tank của Đình hải Plastic để đựng hóa chất HNO3 dùng trong công nghiệp vừa tiết kiệm chi phí, vừa đỡ tốn diện tích.
Nếu các quý khách còn thắc mắc hay cần tư vấn liên hệ theo đường hotline: 0961.247.015 nhân viên của Đình Hải Plastic sẽ tư vấn tận tình cũng như giải đáp thắc mắc cho bạn.
